This article is about the chemical. For its familiar form, common table salt, see Salt. For the medical solutions, see Saline (medicine). For the mineral, see Halite.

Sodium chloride crystals in a form of halite |
|
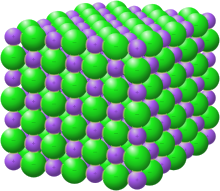
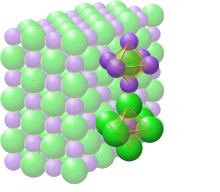
Crystal structure with sodium in purple and chloride in green[1] |
|
| Names | |
|---|---|
| IUPAC name
Sodium chloride |
|
Other names
|
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
|
Beilstein Reference |
3534976 |
| ChEBI |
|
| ChEMBL |
|
| ChemSpider |
|
| ECHA InfoCard | 100.028.726 |
| EC Number |
|
|
Gmelin Reference |
13673 |
| KEGG |
|
| MeSH | Sodium+chloride |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
NaCl |
| Molar mass | 58.443 g/mol[2] |
| Appearance | Colorless cubic crystals[2] |
| Odor | Odorless |
| Density | 2.17 g/cm3[2] |
| Melting point | 800.7 °C (1,473.3 °F; 1,073.8 K)[2] |
| Boiling point | 1,465 °C (2,669 °F; 1,738 K)[2] |
|
Solubility in water |
360 g/1000 g pure water at T = 25 °C[2] |
| Solubility in ammonia | 21.5 g/L at T = ?[clarification needed] |
| Solubility in methanol | 14.9 g/L at T = ?[clarification needed] |
|
Magnetic susceptibility (χ) |
−30.2·10−6 cm3/mol[3] |
|
Refractive index (nD) |
1.5441 (at 589 nm)[4] |
| Structure[5] | |
|
Crystal structure |
Face-centered cubic (see text), cF8 |
|
Space group |
Fm3m (No. 225) |
|
Lattice constant |
a = 564.02 pm |
|
Formula units (Z) |
4 |
|
Coordination geometry |
octahedral at Na+ octahedral at Cl− |
| Thermochemistry[6] | |
|
Heat capacity (C) |
50.5 J/(K·mol) |
|
Std molar |
72.10 J/(K·mol) |
|
Std enthalpy of |
−411.120 kJ/mol |
| Pharmacology | |
|
ATC code |
A12CA01 (WHO) B05CB01 (WHO), B05XA03 (WHO), S01XA03 (WHO) |
| Hazards | |
| NFPA 704 (fire diamond) |
0 0 0 |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
3 g/kg (oral, rats)[7] |
| Related compounds | |
|
Other anions |
Sodium fluoride Sodium bromide Sodium iodide Sodium astatide |
|
Other cations |
Lithium chloride Potassium chloride Rubidium chloride Caesium chloride Francium chloride |
| Supplementary data page | |
| Sodium chloride (data page) | |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Sodium chloride ,[8] commonly known as salt (although sea salt also contains other chemical salts), is an ionic compound with the chemical formula NaCl, representing a 1:1 ratio of sodium and chloride ions. With molar masses of 22.99 and 35.45 g/mol respectively, 100 g of NaCl contains 39.34 g Na and 60.66 g Cl. Sodium chloride is the salt most responsible for the salinity of seawater and of the extracellular fluid of many multicellular organisms. In its edible form, salt (also known as table salt) is commonly used as a condiment and food preservative. Large quantities of sodium chloride are used in many industrial processes, and it is a major source of sodium and chlorine compounds used as feedstocks for further chemical syntheses. Another major application of sodium chloride is de-icing of roadways in sub-freezing weather.
Uses[edit]
In addition to the familiar domestic uses of salt, more dominant applications of the approximately 250 million tonnes per year production (2008 data) include chemicals and de-icing.[9]
Chemical functions[edit]
Salt is used, directly or indirectly, in the production of many chemicals, which consume most of the world’s production.[10]
Chlor-alkali industry[edit]
It is the starting point for the chloralkali process, the industrial process to produce chlorine and sodium hydroxide, according to the chemical equation
This electrolysis is conducted in either a mercury cell, a diaphragm cell, or a membrane cell. Each of those uses a different method to separate the chlorine from the sodium hydroxide. Other technologies are under development due to the high energy consumption of the electrolysis, whereby small improvements in the efficiency can have large economic paybacks. Some applications of chlorine include PVC thermoplastics production, disinfectants, and solvents.
Sodium hydroxide is extensively used in many different industries enabling production of paper, soap, and aluminium etc.
Soda-ash industry[edit]
Sodium chloride is used in the Solvay process to produce sodium carbonate and calcium chloride. Sodium carbonate, in turn, is used to produce glass, sodium bicarbonate, and dyes, as well as a myriad of other chemicals. In the Mannheim process, sodium chloride is used for the production of sodium sulfate and hydrochloric acid.
Standard[edit]
Sodium chloride has an international standard that is created by ASTM International. The standard is named ASTM E534-13 and is the standard test methods for chemical analysis of sodium chloride. These methods listed provide procedures for analyzing sodium chloride to determine whether it is suitable for its intended use and application.
Miscellaneous industrial uses[edit]
Sodium chloride is heavily used, so even relatively minor applications can consume massive quantities. In oil and gas exploration, salt is an important component of drilling fluids in well drilling. It is used to flocculate and increase the density of the drilling fluid to overcome high downwell gas pressures. Whenever a drill hits a salt formation, salt is added to the drilling fluid to saturate the solution in order to minimize the dissolution within the salt stratum.[9] Salt is also used to increase the curing of concrete in cemented casings.[10]
In textiles and dyeing, salt is used as a brine rinse to separate organic contaminants, to promote «salting out» of dyestuff precipitates, and to blend with concentrated dyes to standardize[clarification needed] them. One of its main roles is to provide the positive ion charge to promote the absorption of negatively charged ions of dyes.[10]
It is also used in processing aluminium, beryllium, copper, steel and vanadium. In the pulp and paper industry, salt is used to bleach wood pulp. It also is used to make sodium chlorate, which is added along with sulfuric acid and water to manufacture chlorine dioxide, an excellent oxygen-based bleaching chemical. The chlorine dioxide process, which originated in Germany after World War I, is becoming more popular because of environmental pressures to reduce or eliminate chlorinated bleaching compounds. In tanning and leather treatment, salt is added to animal hides to inhibit microbial activity on the underside of the hides and to attract moisture back into the hides.[10]
In rubber manufacture, salt is used to make buna, neoprene and white rubber types. Salt brine and sulfuric acid are used to coagulate an emulsified latex made from chlorinated butadiene.[10][9]
Salt also is added to secure the soil and to provide firmness to the foundation on which highways are built. The salt acts to minimize the effects of shifting caused in the subsurface by changes in humidity and traffic load.[10]
Sodium chloride is sometimes used as a cheap and safe desiccant because of its hygroscopic properties, making salting an effective method of food preservation historically; the salt draws water out of bacteria through osmotic pressure, keeping it from reproducing, a major source of food spoilage. Even though more effective desiccants are available, few are safe for humans to ingest.
Water softening[edit]
Hard water contains calcium and magnesium ions that interfere with action of soap and contribute to the buildup of a scale or film of alkaline mineral deposits in household and industrial equipment and pipes. Commercial and residential water-softening units use ion-exchange resins to remove ions that cause the hardness. These resins are generated and regenerated using sodium chloride.[10][9]
Road salt[edit]
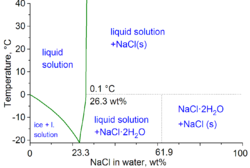
Phase diagram of water–NaCl mixture
The second major application of salt is for de-icing and anti-icing of roads, both in grit bins and spread by winter service vehicles. In anticipation of snowfall, roads are optimally «anti-iced» with brine (concentrated solution of salt in water), which prevents bonding between the snow-ice and the road surface. This procedure obviates the heavy use of salt after the snowfall. For de-icing, mixtures of brine and salt are used, sometimes with additional agents such as calcium chloride and/or magnesium chloride. The use of salt or brine becomes ineffective below −10 °C (14 °F).
Mounds of road salt for use in winter
Salt for de-icing in the United Kingdom predominantly comes from a single mine in Winsford in Cheshire. Prior to distribution it is mixed with <100 ppm of sodium ferrocyanide as an anti-caking agent, which enables rock salt to flow freely out of the gritting vehicles despite being stockpiled prior to use. In recent years this additive has also been used in table salt. Other additives had been used in road salt to reduce the total costs. For example, in the US, a byproduct carbohydrate solution from sugar-beet processing was mixed with rock salt and adhered to road surfaces about 40% better than loose rock salt alone. Because it stayed on the road longer, the treatment did not have to be repeated several times, saving time and money.[10]
In the technical terms of physical chemistry, the minimum freezing point of a water-salt mixture is −21.12 °C (−6.02 °F) for 23.31 wt% of salt. Freezing near this concentration is however so slow that the eutectic point of −22.4 °C (−8.3 °F) can be reached with about 25 wt% of salt.[11]
Environmental effects[edit]
Road salt ends up in fresh-water bodies and could harm aquatic plants and animals by disrupting their osmoregulation ability.[12] The omnipresence of salt poses a problem in any coastal coating application, as trapped salts cause great problems in adhesion. Naval authorities and ship builders monitor the salt concentrations on surfaces during construction. Maximal salt concentrations on surfaces are dependent on the authority and application. The IMO regulation is mostly used and sets salt levels to a maximum of 50 mg/m2 soluble salts measured as sodium chloride. These measurements are done by means of a Bresle test. Salinization (increasing salinity, aka freshwater salinization syndrome) and subsequent increased metal leaching is an ongoing problem throughout North America and European fresh waterways.[13]
In highway de-icing, salt has been associated with corrosion of bridge decks, motor vehicles, reinforcement bar and wire, and unprotected steel structures used in road construction. Surface runoff, vehicle spraying, and windblown actions also affect soil, roadside vegetation, and local surface water and groundwater supplies. Although evidence of environmental loading of salt has been found during peak usage, the spring rains and thaws usually dilute the concentrations of sodium in the area where salt was applied.[10] A 2009 study found that approximately 70% of the road salt being applied in the Minneapolis-St Paul metro area is retained in the local watershed.[14]
Substitution[edit]
Some agencies are substituting beer, molasses, and beet juice instead of road salt.[15] Airlines utilize more glycol and sugar rather than salt based solutions for de-icing.[16]
Food industry and agriculture[edit]
Main article: Salt
Many microorganisms cannot live in a salty environment: water is drawn out of their cells by osmosis. For this reason salt is used to preserve some foods, such as bacon, fish, or cabbage.
Salt is added to food, either by the food producer or by the consumer, as a flavor enhancer, preservative, binder, fermentation-control additive, texture-control agent and color developer. The salt consumption in the food industry is subdivided, in descending order of consumption, into other food processing, meat packers, canning, baking, dairy and grain mill products. Salt is added to promote color development in bacon, ham and other processed meat products. As a preservative, salt inhibits the growth of bacteria. Salt acts as a binder in sausages to form a binding gel made up of meat, fat, and moisture. Salt also acts as a flavor enhancer and as a tenderizer.[10]
In many dairy industries, salt is added to cheese as a color-, fermentation-, and texture-control agent. The dairy subsector includes companies that manufacture creamery butter, condensed and evaporated milk, frozen desserts, ice cream, natural and processed cheese, and specialty dairy products. In canning, salt is primarily added as a flavor enhancer and preservative. It also is used as a carrier for other ingredients, dehydrating agent, enzyme inhibitor and tenderizer. In baking, salt is added to control the rate of fermentation in bread dough. It also is used to strengthen the gluten (the elastic protein-water complex in certain doughs) and as a flavor enhancer, such as a topping on baked goods. The food-processing category also contains grain mill products. These products consist of milling flour and rice and manufacturing cereal breakfast food and blended or prepared flour. Salt is also used a seasoning agent, e.g. in potato chips, pretzels, cat and dog food.[10]
Sodium chloride is used in veterinary medicine as emesis-causing agent. It is given as warm saturated solution. Emesis can also be caused by pharyngeal placement of small amount of plain salt or salt crystals.
Medicine[edit]
Sodium chloride is used together with water as one of the primary solutions for intravenous therapy. Nasal spray often contains a saline solution.
Firefighting[edit]
A class-D fire extinguisher for various metals
Sodium chloride is the principal extinguishing agent in fire extinguishers (Met-L-X, Super D) used on combustible metal fires such as magnesium, potassium, sodium, and NaK alloys (Class D). Thermoplastic powder is added to the mixture, along with waterproofing (metal stearates) and anti-caking materials (tricalcium phosphate) to form the extinguishing agent. When it is applied to the fire, the salt acts like a heat sink, dissipating heat from the fire, and also forms an oxygen-excluding crust to smother the fire. The plastic additive melts and helps the crust maintain its integrity until the burning metal cools below its ignition temperature. This type of extinguisher was invented in the late 1940s as a cartridge-operated unit, although stored pressure versions are now popular. Common sizes are 30 pounds (14 kg) portable and 350 pounds (160 kg) wheeled.[citation needed]
Cleanser[edit]
Since at least medieval times, people have used salt as a cleansing agent rubbed on household surfaces. It is also used in many brands of shampoo, toothpaste and popularly to de-ice driveways and patches of ice.
Optical usage[edit]
Defect-free NaCl crystals have an optical transmittance of about 90% for infrared light, specifically between 200 nm and 20 µm. They were therefore used in optical components (windows and prisms) operating in that spectral range, where few non-absorbing alternatives exist and where requirements for absence of microscopic inhomogeneities are less strict than in the visible range. While inexpensive, NaCl crystals are soft and hygroscopic – when exposed to the ambient air, they gradually cover with «frost». This limits application of NaCl to dry environments, vacuum sealed assembly areas or for short-term uses such as prototyping. Nowadays materials like zinc selenide (ZnSe), which are stronger mechanically and are less sensitive to moisture, are used instead of NaCl for the infrared spectral range.
Chemistry[edit]
Solid sodium chloride[edit]
Sodium chloride crystal under microscope.
NaCl octahedra. The yellow stipples represent the electrostatic force between the ions of opposite charge
In solid sodium chloride, each ion is surrounded by six ions of the opposite charge as expected on electrostatic grounds. The surrounding ions are located at the vertices of a regular octahedron. In the language of close-packing, the larger chloride ions (167 pm in size[17]) are arranged in a cubic array whereas the smaller sodium ions (116 pm[17]) fill all the cubic gaps (octahedral voids) between them. This same basic structure is found in many other compounds and is commonly known as the halite or rock-salt crystal structure. It can be represented as a face-centered cubic (fcc) lattice with a two-atom basis or as two interpenetrating face centered cubic lattices. The first atom is located at each lattice point, and the second atom is located halfway between lattice points along the fcc unit cell edge.
Solid sodium chloride has a melting point of 801 °C. Thermal conductivity of sodium chloride as a function of temperature has a maximum of 2.03 W/(cm K) at 8 K (−265.15 °C; −445.27 °F) and decreases to 0.069 at 314 K (41 °C; 106 °F). It also decreases with doping.[18]
Atomic-resolution real-time video imaging allows visualization of the initial stage of crystal nucleation of sodium chloride.[19]
Aqueous solutions[edit]
| Solubility of NaCl (g NaCl / 1 kg of solvent at 25 °C (77 °F))[20] |
|
|---|---|
| Water | 360 |
| Formamide | 94 |
| Glycerin | 83 |
| Propylene glycol | 71 |
| Formic acid | 52 |
| Liquid ammonia | 30.2 |
| Methanol | 14 |
| Ethanol | 0.65 |
| Dimethylformamide | 0.4 |
| Propan-1-ol | 0.124 |
| Sulfolane | 0.05 |
| Butan-1-ol | 0.05 |
| Propan-2-ol | 0.03 |
| Pentan-1-ol | 0.018 |
| Acetonitrile | 0.003 |
| Acetone | 0.00042 |
The attraction between the Na+ and Cl− ions in the solid is so strong that only highly polar solvents like water dissolve NaCl well.
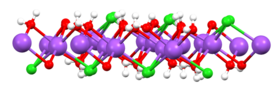
View of one slab of NaCl(H2O)2 (red = O, white = H, green = Cl, purple = Na).[21]
When dissolved in water, the sodium chloride framework disintegrates as the Na+ and Cl− ions become surrounded by polar water molecules. These solutions consist of metal aquo complex with the formula [Na(H2O)8]+, with the Na–O distance of 250 pm. The chloride ions are also strongly solvated, each being surrounded by an average of six molecules of water.[22] Solutions of sodium chloride have very different properties from pure water. The eutectic point is −21.12 °C (−6.02 °F) for 23.31% mass fraction of salt, and the boiling point of saturated salt solution is near 108.7 °C (227.7 °F).[11] From cold solutions, salt crystallises as the dihydrate NaCl·2H2O.[23]
pH of sodium chloride solutions[edit]
The pH of a sodium chloride solution remains ≈7 due to the extremely weak basicity of the Cl− ion, which is the conjugate base of the strong acid HCl. In other words, NaCl has no effect on system pH[24] in diluted solutions where the effects of ionic strength and activity coefficients are negligible.
Stoichiometric and structure variants[edit]
Common salt has a 1:1 molar ratio of sodium and chlorine. In 2013, compounds of sodium and chloride of different stoichiometries have been discovered; five new compounds were predicted (e.g., Na3Cl, Na2Cl, Na3Cl2, NaCl3, and NaCl7). The existence of some of them has been experimentally confirmed at high pressures: cubic and orthorhombic NaCl3 and two-dimensional metallic tetragonal Na3Cl. This indicates that compounds violating chemical intuition are possible, in simple systems under nonambient conditions.[25]
Occurrence[edit]
Most of the world’s salt is dissolved in the ocean[citation needed]. A lesser amount is found in the Earth’s crust as the water-soluble mineral halite (rock salt), and a tiny amount exists as suspended sea salt particles in the atmosphere[citation needed]. These particles are the dominant cloud condensation nuclei far out at sea, which allow the formation of clouds in otherwise non-polluted air.[26]
Production[edit]
Salt is currently mass-produced by evaporation of seawater or brine from brine wells and salt lakes. Mining of rock salt is also a major source. China is the world’s main supplier of salt.[10] In 2017, world production was estimated at 280 million tonnes, the top five producers (in million tonnes) being China (68.0), United States (43.0), India (26.0), Germany (13.0), and Canada (13.0).[27] Salt is also a byproduct of potassium mining.
See also[edit]
- Biosalinity
- Edible salt (table salt)
- Halite, the mineral form of sodium chloride
- Health effects of salt
- Salinity
- Salting the earth
- Salt poisoning
References[edit]
- ^ «Sodium Chloride (NaCl) Crystal». PhysicsOpenLab. Retrieved 23 August 2021.
- ^ a b c d e f Haynes, 4.89
- ^ Haynes, 4.135
- ^ Haynes, 10.241
- ^ Haynes, 4.148
- ^ Haynes, 5.8
- ^ Sodium chloride. nlm.nih.gov.
- ^ Wells, John C. (2008), Longman Pronunciation Dictionary (3rd ed.), Longman, pp. 143 and 755, ISBN 9781405881180
- ^ a b c d Westphal, Gisbert et al. (2002) «Sodium Chloride» in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim doi:10.1002/14356007.a24_317.pub4.
- ^ a b c d e f g h i j k l Kostick, Dennis S. (October 2010) «Salt» in U.S. Geological Survey, 2008 Minerals Yearbook
- ^ a b Elvers, B. et al. (ed.) (1991) Ullmann’s Encyclopedia of Industrial Chemistry, 5th ed. Vol. A24, Wiley, p. 319, ISBN 978-3-527-20124-2.
- ^ Rastogi, Nina (16 February 2010) Does road salt harm the environment? slate.com.
- ^ «Saltier waterways are creating dangerous ‘chemical cocktails’«. phys.org.
- ^ «Most Road Salt Is Making It into Lakes And Rivers». www.sciencedaily.com. University of Minnesota. 20 February 2009. Retrieved 27 September 2015.
- ^ Casey, Michael. «Turning to beet juice and beer to address road salt danger». phys.org.
- ^ «EASA Cautions on Organic Salt Deicing Fluid». MRO Network. 9 December 2016.
- ^ a b R. D. Shannon (1976). «Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides». Acta Crystallogr A. 32 (5): 751–767. Bibcode:1976AcCrA..32..751S. doi:10.1107/S0567739476001551.
- ^ Sirdeshmukh, Dinker B.; Sirdeshmukh, Lalitha & Subhadra, K. G. (2001). Alkali halides: a handbook of physical properties. Springer. pp. 65, 68. ISBN 978-3-540-42180-1.
- ^ Nakamuro, Takayuki; Sakakibara, Masaya; Nada, Hiroki; Harano, Koji; Nakamura, Eiichi (2021). «Capturing the Moment of Emergence of Crystal Nucleus from Disorder». Journal of the American Chemical Society. 143 (4): 1763–1767. doi:10.1021/jacs.0c12100. PMID 33475359.
- ^ Burgess, J (1978). Metal Ions in Solution. New York: Ellis Horwood. ISBN 978-0-85312-027-8.
- ^ Klewe, B; Pedersen (1974). «The crystal structure of sodium chloride dihydrate». Acta Crystallogr. B30 (10): 2363–2371. doi:10.1107/S0567740874007138.
- ^ Lincoln, S. F.; Richens, D. T. and Sykes, A. G. (2003) «Metal Aqua Ions» Comprehensive Coordination Chemistry II Volume 1, pp. 515–555. doi:10.1016/B0-08-043748-6/01055-0.
- ^ Water-NaCl phase diagram. Lide, CRC Handbook of Chemistry and Physics, 86 ed (2005-2006), CRC pages 8-71, 8-116
- ^ «Acidic, Basic, and Neutral Salts». Flinn Scientific Chem Fax. 2016. Retrieved 18 September 2018.
Neutralization of a strong acid and a strong base gives a neutral salt.
- ^ Zhang, W.; Oganov, A. R.; Goncharov, A. F.; Zhu, Q.; Boulfelfel, S. E.; Lyakhov, A. O.; Stavrou, E.; Somayazulu, M.; Prakapenka, V. B.; Konôpková, Z. (2013). «Unexpected Stable Stoichiometries of Sodium Chlorides». Science. 342 (6165): 1502–1505. arXiv:1310.7674. Bibcode:2013Sci…342.1502Z. doi:10.1126/science.1244989. PMID 24357316. S2CID 15298372.
- ^ Mason, B. J. (2006). «The role of sea-salt particles as cloud condensation nuclei over the remote oceans». Quarterly Journal of the Royal Meteorological Society. 127 (576): 2023–32. Bibcode:2001QJRMS.127.2023M. doi:10.1002/qj.49712757609. S2CID 121846285.
- ^ Salt, U.S. Geological Survey
This article incorporates public domain material from Salt (PDF). United States Geological Survey.
Cited sources[edit]
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. ISBN 978-1439855119.
External links[edit]
Wikimedia Commons has media related to NaCl.
- Salt United States Geological Survey Statistics and Information
- «Using Salt and Sand for Winter Road Maintenance». Road Management Journal. December 1997. Archived from the original on 21 September 2016. Retrieved 13 February 2007.
- Calculators: surface tensions, and densities, molarities and molalities of aqueous NaCl (and other salts)
- JtBaker MSDS
This article is about the chemical. For its familiar form, common table salt, see Salt. For the medical solutions, see Saline (medicine). For the mineral, see Halite.

Sodium chloride crystals in a form of halite |
|

Crystal structure with sodium in purple and chloride in green[1] |
|
| Names | |
|---|---|
| IUPAC name
Sodium chloride |
|
Other names
|
|
| Identifiers | |
|
CAS Number |
|
|
3D model (JSmol) |
|
|
Beilstein Reference |
3534976 |
| ChEBI |
|
| ChEMBL |
|
| ChemSpider |
|
| ECHA InfoCard | 100.028.726 |
| EC Number |
|
|
Gmelin Reference |
13673 |
| KEGG |
|
| MeSH | Sodium+chloride |
|
PubChem CID |
|
| RTECS number |
|
| UNII |
|
|
CompTox Dashboard (EPA) |
|
|
InChI
|
|
|
SMILES
|
|
| Properties | |
|
Chemical formula |
NaCl |
| Molar mass | 58.443 g/mol[2] |
| Appearance | Colorless cubic crystals[2] |
| Odor | Odorless |
| Density | 2.17 g/cm3[2] |
| Melting point | 800.7 °C (1,473.3 °F; 1,073.8 K)[2] |
| Boiling point | 1,465 °C (2,669 °F; 1,738 K)[2] |
|
Solubility in water |
360 g/1000 g pure water at T = 25 °C[2] |
| Solubility in ammonia | 21.5 g/L at T = ?[clarification needed] |
| Solubility in methanol | 14.9 g/L at T = ?[clarification needed] |
|
Magnetic susceptibility (χ) |
−30.2·10−6 cm3/mol[3] |
|
Refractive index (nD) |
1.5441 (at 589 nm)[4] |
| Structure[5] | |
|
Crystal structure |
Face-centered cubic (see text), cF8 |
|
Space group |
Fm3m (No. 225) |
|
Lattice constant |
a = 564.02 pm |
|
Formula units (Z) |
4 |
|
Coordination geometry |
octahedral at Na+ octahedral at Cl− |
| Thermochemistry[6] | |
|
Heat capacity (C) |
50.5 J/(K·mol) |
|
Std molar |
72.10 J/(K·mol) |
|
Std enthalpy of |
−411.120 kJ/mol |
| Pharmacology | |
|
ATC code |
A12CA01 (WHO) B05CB01 (WHO), B05XA03 (WHO), S01XA03 (WHO) |
| Hazards | |
| NFPA 704 (fire diamond) |
0 0 0 |
| Lethal dose or concentration (LD, LC): | |
|
LD50 (median dose) |
3 g/kg (oral, rats)[7] |
| Related compounds | |
|
Other anions |
Sodium fluoride Sodium bromide Sodium iodide Sodium astatide |
|
Other cations |
Lithium chloride Potassium chloride Rubidium chloride Caesium chloride Francium chloride |
| Supplementary data page | |
| Sodium chloride (data page) | |
|
Except where otherwise noted, data are given for materials in their standard state (at 25 °C [77 °F], 100 kPa).
Infobox references |
Sodium chloride ,[8] commonly known as salt (although sea salt also contains other chemical salts), is an ionic compound with the chemical formula NaCl, representing a 1:1 ratio of sodium and chloride ions. With molar masses of 22.99 and 35.45 g/mol respectively, 100 g of NaCl contains 39.34 g Na and 60.66 g Cl. Sodium chloride is the salt most responsible for the salinity of seawater and of the extracellular fluid of many multicellular organisms. In its edible form, salt (also known as table salt) is commonly used as a condiment and food preservative. Large quantities of sodium chloride are used in many industrial processes, and it is a major source of sodium and chlorine compounds used as feedstocks for further chemical syntheses. Another major application of sodium chloride is de-icing of roadways in sub-freezing weather.
Uses[edit]
In addition to the familiar domestic uses of salt, more dominant applications of the approximately 250 million tonnes per year production (2008 data) include chemicals and de-icing.[9]
Chemical functions[edit]
Salt is used, directly or indirectly, in the production of many chemicals, which consume most of the world’s production.[10]
Chlor-alkali industry[edit]
It is the starting point for the chloralkali process, the industrial process to produce chlorine and sodium hydroxide, according to the chemical equation
This electrolysis is conducted in either a mercury cell, a diaphragm cell, or a membrane cell. Each of those uses a different method to separate the chlorine from the sodium hydroxide. Other technologies are under development due to the high energy consumption of the electrolysis, whereby small improvements in the efficiency can have large economic paybacks. Some applications of chlorine include PVC thermoplastics production, disinfectants, and solvents.
Sodium hydroxide is extensively used in many different industries enabling production of paper, soap, and aluminium etc.
Soda-ash industry[edit]
Sodium chloride is used in the Solvay process to produce sodium carbonate and calcium chloride. Sodium carbonate, in turn, is used to produce glass, sodium bicarbonate, and dyes, as well as a myriad of other chemicals. In the Mannheim process, sodium chloride is used for the production of sodium sulfate and hydrochloric acid.
Standard[edit]
Sodium chloride has an international standard that is created by ASTM International. The standard is named ASTM E534-13 and is the standard test methods for chemical analysis of sodium chloride. These methods listed provide procedures for analyzing sodium chloride to determine whether it is suitable for its intended use and application.
Miscellaneous industrial uses[edit]
Sodium chloride is heavily used, so even relatively minor applications can consume massive quantities. In oil and gas exploration, salt is an important component of drilling fluids in well drilling. It is used to flocculate and increase the density of the drilling fluid to overcome high downwell gas pressures. Whenever a drill hits a salt formation, salt is added to the drilling fluid to saturate the solution in order to minimize the dissolution within the salt stratum.[9] Salt is also used to increase the curing of concrete in cemented casings.[10]
In textiles and dyeing, salt is used as a brine rinse to separate organic contaminants, to promote «salting out» of dyestuff precipitates, and to blend with concentrated dyes to standardize[clarification needed] them. One of its main roles is to provide the positive ion charge to promote the absorption of negatively charged ions of dyes.[10]
It is also used in processing aluminium, beryllium, copper, steel and vanadium. In the pulp and paper industry, salt is used to bleach wood pulp. It also is used to make sodium chlorate, which is added along with sulfuric acid and water to manufacture chlorine dioxide, an excellent oxygen-based bleaching chemical. The chlorine dioxide process, which originated in Germany after World War I, is becoming more popular because of environmental pressures to reduce or eliminate chlorinated bleaching compounds. In tanning and leather treatment, salt is added to animal hides to inhibit microbial activity on the underside of the hides and to attract moisture back into the hides.[10]
In rubber manufacture, salt is used to make buna, neoprene and white rubber types. Salt brine and sulfuric acid are used to coagulate an emulsified latex made from chlorinated butadiene.[10][9]
Salt also is added to secure the soil and to provide firmness to the foundation on which highways are built. The salt acts to minimize the effects of shifting caused in the subsurface by changes in humidity and traffic load.[10]
Sodium chloride is sometimes used as a cheap and safe desiccant because of its hygroscopic properties, making salting an effective method of food preservation historically; the salt draws water out of bacteria through osmotic pressure, keeping it from reproducing, a major source of food spoilage. Even though more effective desiccants are available, few are safe for humans to ingest.
Water softening[edit]
Hard water contains calcium and magnesium ions that interfere with action of soap and contribute to the buildup of a scale or film of alkaline mineral deposits in household and industrial equipment and pipes. Commercial and residential water-softening units use ion-exchange resins to remove ions that cause the hardness. These resins are generated and regenerated using sodium chloride.[10][9]
Road salt[edit]
Phase diagram of water–NaCl mixture
The second major application of salt is for de-icing and anti-icing of roads, both in grit bins and spread by winter service vehicles. In anticipation of snowfall, roads are optimally «anti-iced» with brine (concentrated solution of salt in water), which prevents bonding between the snow-ice and the road surface. This procedure obviates the heavy use of salt after the snowfall. For de-icing, mixtures of brine and salt are used, sometimes with additional agents such as calcium chloride and/or magnesium chloride. The use of salt or brine becomes ineffective below −10 °C (14 °F).
Mounds of road salt for use in winter
Salt for de-icing in the United Kingdom predominantly comes from a single mine in Winsford in Cheshire. Prior to distribution it is mixed with <100 ppm of sodium ferrocyanide as an anti-caking agent, which enables rock salt to flow freely out of the gritting vehicles despite being stockpiled prior to use. In recent years this additive has also been used in table salt. Other additives had been used in road salt to reduce the total costs. For example, in the US, a byproduct carbohydrate solution from sugar-beet processing was mixed with rock salt and adhered to road surfaces about 40% better than loose rock salt alone. Because it stayed on the road longer, the treatment did not have to be repeated several times, saving time and money.[10]
In the technical terms of physical chemistry, the minimum freezing point of a water-salt mixture is −21.12 °C (−6.02 °F) for 23.31 wt% of salt. Freezing near this concentration is however so slow that the eutectic point of −22.4 °C (−8.3 °F) can be reached with about 25 wt% of salt.[11]
Environmental effects[edit]
Road salt ends up in fresh-water bodies and could harm aquatic plants and animals by disrupting their osmoregulation ability.[12] The omnipresence of salt poses a problem in any coastal coating application, as trapped salts cause great problems in adhesion. Naval authorities and ship builders monitor the salt concentrations on surfaces during construction. Maximal salt concentrations on surfaces are dependent on the authority and application. The IMO regulation is mostly used and sets salt levels to a maximum of 50 mg/m2 soluble salts measured as sodium chloride. These measurements are done by means of a Bresle test. Salinization (increasing salinity, aka freshwater salinization syndrome) and subsequent increased metal leaching is an ongoing problem throughout North America and European fresh waterways.[13]
In highway de-icing, salt has been associated with corrosion of bridge decks, motor vehicles, reinforcement bar and wire, and unprotected steel structures used in road construction. Surface runoff, vehicle spraying, and windblown actions also affect soil, roadside vegetation, and local surface water and groundwater supplies. Although evidence of environmental loading of salt has been found during peak usage, the spring rains and thaws usually dilute the concentrations of sodium in the area where salt was applied.[10] A 2009 study found that approximately 70% of the road salt being applied in the Minneapolis-St Paul metro area is retained in the local watershed.[14]
Substitution[edit]
Some agencies are substituting beer, molasses, and beet juice instead of road salt.[15] Airlines utilize more glycol and sugar rather than salt based solutions for de-icing.[16]
Food industry and agriculture[edit]
Main article: Salt
Many microorganisms cannot live in a salty environment: water is drawn out of their cells by osmosis. For this reason salt is used to preserve some foods, such as bacon, fish, or cabbage.
Salt is added to food, either by the food producer or by the consumer, as a flavor enhancer, preservative, binder, fermentation-control additive, texture-control agent and color developer. The salt consumption in the food industry is subdivided, in descending order of consumption, into other food processing, meat packers, canning, baking, dairy and grain mill products. Salt is added to promote color development in bacon, ham and other processed meat products. As a preservative, salt inhibits the growth of bacteria. Salt acts as a binder in sausages to form a binding gel made up of meat, fat, and moisture. Salt also acts as a flavor enhancer and as a tenderizer.[10]
In many dairy industries, salt is added to cheese as a color-, fermentation-, and texture-control agent. The dairy subsector includes companies that manufacture creamery butter, condensed and evaporated milk, frozen desserts, ice cream, natural and processed cheese, and specialty dairy products. In canning, salt is primarily added as a flavor enhancer and preservative. It also is used as a carrier for other ingredients, dehydrating agent, enzyme inhibitor and tenderizer. In baking, salt is added to control the rate of fermentation in bread dough. It also is used to strengthen the gluten (the elastic protein-water complex in certain doughs) and as a flavor enhancer, such as a topping on baked goods. The food-processing category also contains grain mill products. These products consist of milling flour and rice and manufacturing cereal breakfast food and blended or prepared flour. Salt is also used a seasoning agent, e.g. in potato chips, pretzels, cat and dog food.[10]
Sodium chloride is used in veterinary medicine as emesis-causing agent. It is given as warm saturated solution. Emesis can also be caused by pharyngeal placement of small amount of plain salt or salt crystals.
Medicine[edit]
Sodium chloride is used together with water as one of the primary solutions for intravenous therapy. Nasal spray often contains a saline solution.
Firefighting[edit]
A class-D fire extinguisher for various metals
Sodium chloride is the principal extinguishing agent in fire extinguishers (Met-L-X, Super D) used on combustible metal fires such as magnesium, potassium, sodium, and NaK alloys (Class D). Thermoplastic powder is added to the mixture, along with waterproofing (metal stearates) and anti-caking materials (tricalcium phosphate) to form the extinguishing agent. When it is applied to the fire, the salt acts like a heat sink, dissipating heat from the fire, and also forms an oxygen-excluding crust to smother the fire. The plastic additive melts and helps the crust maintain its integrity until the burning metal cools below its ignition temperature. This type of extinguisher was invented in the late 1940s as a cartridge-operated unit, although stored pressure versions are now popular. Common sizes are 30 pounds (14 kg) portable and 350 pounds (160 kg) wheeled.[citation needed]
Cleanser[edit]
Since at least medieval times, people have used salt as a cleansing agent rubbed on household surfaces. It is also used in many brands of shampoo, toothpaste and popularly to de-ice driveways and patches of ice.
Optical usage[edit]
Defect-free NaCl crystals have an optical transmittance of about 90% for infrared light, specifically between 200 nm and 20 µm. They were therefore used in optical components (windows and prisms) operating in that spectral range, where few non-absorbing alternatives exist and where requirements for absence of microscopic inhomogeneities are less strict than in the visible range. While inexpensive, NaCl crystals are soft and hygroscopic – when exposed to the ambient air, they gradually cover with «frost». This limits application of NaCl to dry environments, vacuum sealed assembly areas or for short-term uses such as prototyping. Nowadays materials like zinc selenide (ZnSe), which are stronger mechanically and are less sensitive to moisture, are used instead of NaCl for the infrared spectral range.
Chemistry[edit]
Solid sodium chloride[edit]
Sodium chloride crystal under microscope.
NaCl octahedra. The yellow stipples represent the electrostatic force between the ions of opposite charge
In solid sodium chloride, each ion is surrounded by six ions of the opposite charge as expected on electrostatic grounds. The surrounding ions are located at the vertices of a regular octahedron. In the language of close-packing, the larger chloride ions (167 pm in size[17]) are arranged in a cubic array whereas the smaller sodium ions (116 pm[17]) fill all the cubic gaps (octahedral voids) between them. This same basic structure is found in many other compounds and is commonly known as the halite or rock-salt crystal structure. It can be represented as a face-centered cubic (fcc) lattice with a two-atom basis or as two interpenetrating face centered cubic lattices. The first atom is located at each lattice point, and the second atom is located halfway between lattice points along the fcc unit cell edge.
Solid sodium chloride has a melting point of 801 °C. Thermal conductivity of sodium chloride as a function of temperature has a maximum of 2.03 W/(cm K) at 8 K (−265.15 °C; −445.27 °F) and decreases to 0.069 at 314 K (41 °C; 106 °F). It also decreases with doping.[18]
Atomic-resolution real-time video imaging allows visualization of the initial stage of crystal nucleation of sodium chloride.[19]
Aqueous solutions[edit]
| Solubility of NaCl (g NaCl / 1 kg of solvent at 25 °C (77 °F))[20] |
|
|---|---|
| Water | 360 |
| Formamide | 94 |
| Glycerin | 83 |
| Propylene glycol | 71 |
| Formic acid | 52 |
| Liquid ammonia | 30.2 |
| Methanol | 14 |
| Ethanol | 0.65 |
| Dimethylformamide | 0.4 |
| Propan-1-ol | 0.124 |
| Sulfolane | 0.05 |
| Butan-1-ol | 0.05 |
| Propan-2-ol | 0.03 |
| Pentan-1-ol | 0.018 |
| Acetonitrile | 0.003 |
| Acetone | 0.00042 |
The attraction between the Na+ and Cl− ions in the solid is so strong that only highly polar solvents like water dissolve NaCl well.
View of one slab of NaCl(H2O)2 (red = O, white = H, green = Cl, purple = Na).[21]
When dissolved in water, the sodium chloride framework disintegrates as the Na+ and Cl− ions become surrounded by polar water molecules. These solutions consist of metal aquo complex with the formula [Na(H2O)8]+, with the Na–O distance of 250 pm. The chloride ions are also strongly solvated, each being surrounded by an average of six molecules of water.[22] Solutions of sodium chloride have very different properties from pure water. The eutectic point is −21.12 °C (−6.02 °F) for 23.31% mass fraction of salt, and the boiling point of saturated salt solution is near 108.7 °C (227.7 °F).[11] From cold solutions, salt crystallises as the dihydrate NaCl·2H2O.[23]
pH of sodium chloride solutions[edit]
The pH of a sodium chloride solution remains ≈7 due to the extremely weak basicity of the Cl− ion, which is the conjugate base of the strong acid HCl. In other words, NaCl has no effect on system pH[24] in diluted solutions where the effects of ionic strength and activity coefficients are negligible.
Stoichiometric and structure variants[edit]
Common salt has a 1:1 molar ratio of sodium and chlorine. In 2013, compounds of sodium and chloride of different stoichiometries have been discovered; five new compounds were predicted (e.g., Na3Cl, Na2Cl, Na3Cl2, NaCl3, and NaCl7). The existence of some of them has been experimentally confirmed at high pressures: cubic and orthorhombic NaCl3 and two-dimensional metallic tetragonal Na3Cl. This indicates that compounds violating chemical intuition are possible, in simple systems under nonambient conditions.[25]
Occurrence[edit]
Most of the world’s salt is dissolved in the ocean[citation needed]. A lesser amount is found in the Earth’s crust as the water-soluble mineral halite (rock salt), and a tiny amount exists as suspended sea salt particles in the atmosphere[citation needed]. These particles are the dominant cloud condensation nuclei far out at sea, which allow the formation of clouds in otherwise non-polluted air.[26]
Production[edit]
Salt is currently mass-produced by evaporation of seawater or brine from brine wells and salt lakes. Mining of rock salt is also a major source. China is the world’s main supplier of salt.[10] In 2017, world production was estimated at 280 million tonnes, the top five producers (in million tonnes) being China (68.0), United States (43.0), India (26.0), Germany (13.0), and Canada (13.0).[27] Salt is also a byproduct of potassium mining.
See also[edit]
- Biosalinity
- Edible salt (table salt)
- Halite, the mineral form of sodium chloride
- Health effects of salt
- Salinity
- Salting the earth
- Salt poisoning
References[edit]
- ^ «Sodium Chloride (NaCl) Crystal». PhysicsOpenLab. Retrieved 23 August 2021.
- ^ a b c d e f Haynes, 4.89
- ^ Haynes, 4.135
- ^ Haynes, 10.241
- ^ Haynes, 4.148
- ^ Haynes, 5.8
- ^ Sodium chloride. nlm.nih.gov.
- ^ Wells, John C. (2008), Longman Pronunciation Dictionary (3rd ed.), Longman, pp. 143 and 755, ISBN 9781405881180
- ^ a b c d Westphal, Gisbert et al. (2002) «Sodium Chloride» in Ullmann’s Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim doi:10.1002/14356007.a24_317.pub4.
- ^ a b c d e f g h i j k l Kostick, Dennis S. (October 2010) «Salt» in U.S. Geological Survey, 2008 Minerals Yearbook
- ^ a b Elvers, B. et al. (ed.) (1991) Ullmann’s Encyclopedia of Industrial Chemistry, 5th ed. Vol. A24, Wiley, p. 319, ISBN 978-3-527-20124-2.
- ^ Rastogi, Nina (16 February 2010) Does road salt harm the environment? slate.com.
- ^ «Saltier waterways are creating dangerous ‘chemical cocktails’«. phys.org.
- ^ «Most Road Salt Is Making It into Lakes And Rivers». www.sciencedaily.com. University of Minnesota. 20 February 2009. Retrieved 27 September 2015.
- ^ Casey, Michael. «Turning to beet juice and beer to address road salt danger». phys.org.
- ^ «EASA Cautions on Organic Salt Deicing Fluid». MRO Network. 9 December 2016.
- ^ a b R. D. Shannon (1976). «Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides». Acta Crystallogr A. 32 (5): 751–767. Bibcode:1976AcCrA..32..751S. doi:10.1107/S0567739476001551.
- ^ Sirdeshmukh, Dinker B.; Sirdeshmukh, Lalitha & Subhadra, K. G. (2001). Alkali halides: a handbook of physical properties. Springer. pp. 65, 68. ISBN 978-3-540-42180-1.
- ^ Nakamuro, Takayuki; Sakakibara, Masaya; Nada, Hiroki; Harano, Koji; Nakamura, Eiichi (2021). «Capturing the Moment of Emergence of Crystal Nucleus from Disorder». Journal of the American Chemical Society. 143 (4): 1763–1767. doi:10.1021/jacs.0c12100. PMID 33475359.
- ^ Burgess, J (1978). Metal Ions in Solution. New York: Ellis Horwood. ISBN 978-0-85312-027-8.
- ^ Klewe, B; Pedersen (1974). «The crystal structure of sodium chloride dihydrate». Acta Crystallogr. B30 (10): 2363–2371. doi:10.1107/S0567740874007138.
- ^ Lincoln, S. F.; Richens, D. T. and Sykes, A. G. (2003) «Metal Aqua Ions» Comprehensive Coordination Chemistry II Volume 1, pp. 515–555. doi:10.1016/B0-08-043748-6/01055-0.
- ^ Water-NaCl phase diagram. Lide, CRC Handbook of Chemistry and Physics, 86 ed (2005-2006), CRC pages 8-71, 8-116
- ^ «Acidic, Basic, and Neutral Salts». Flinn Scientific Chem Fax. 2016. Retrieved 18 September 2018.
Neutralization of a strong acid and a strong base gives a neutral salt.
- ^ Zhang, W.; Oganov, A. R.; Goncharov, A. F.; Zhu, Q.; Boulfelfel, S. E.; Lyakhov, A. O.; Stavrou, E.; Somayazulu, M.; Prakapenka, V. B.; Konôpková, Z. (2013). «Unexpected Stable Stoichiometries of Sodium Chlorides». Science. 342 (6165): 1502–1505. arXiv:1310.7674. Bibcode:2013Sci…342.1502Z. doi:10.1126/science.1244989. PMID 24357316. S2CID 15298372.
- ^ Mason, B. J. (2006). «The role of sea-salt particles as cloud condensation nuclei over the remote oceans». Quarterly Journal of the Royal Meteorological Society. 127 (576): 2023–32. Bibcode:2001QJRMS.127.2023M. doi:10.1002/qj.49712757609. S2CID 121846285.
- ^ Salt, U.S. Geological Survey
This article incorporates public domain material from Salt (PDF). United States Geological Survey.
Cited sources[edit]
- Haynes, William M., ed. (2011). CRC Handbook of Chemistry and Physics (92nd ed.). CRC Press. ISBN 978-1439855119.
External links[edit]
Wikimedia Commons has media related to NaCl.
- Salt United States Geological Survey Statistics and Information
- «Using Salt and Sand for Winter Road Maintenance». Road Management Journal. December 1997. Archived from the original on 21 September 2016. Retrieved 13 February 2007.
- Calculators: surface tensions, and densities, molarities and molalities of aqueous NaCl (and other salts)
- JtBaker MSDS
Содержание
- Структурная формула
- Русское название
- Английское название
- Латинское название вещества Натрия хлорид
- Брутто формула
- Фармакологическая группа вещества Натрия хлорид
- Нозологическая классификация
- Код CAS
- Фармакологическое действие
- Характеристика
- Фармакология
- Применение вещества Натрия хлорид
- Противопоказания
- Ограничения к применению
- Побочные действия вещества Натрия хлорид
- Передозировка
- Способ применения и дозы
- Торговые названия с действующим веществом Натрия хлорид
Структурная формула
Русское название
Натрия хлорид
Английское название
Sodium chloride
Латинское название вещества Натрия хлорид
Natrii chloridum (род. Natrii chloridi)
Фармакологическая группа вещества Натрия хлорид
Нозологическая классификация
Список кодов МКБ-10
- K92.2 Желудочно-кишечное кровотечение неуточненное
- K52.1 Токсический гастроэнтерит и колит
- T79.3 Посттравматическая раневая инфекция, не классифицированная в других рубриках
- K30 Диспепсия
- E87.1 Гипоосмолярность и гипонатриемия
- E86 Уменьшение объема жидкости [гиповолемия]
- T30 Термические и химические ожоги неуточненной локализации
- R58 Кровотечение, не классифицированное в других рубриках
- T57.8 Других уточненных неорганических веществ
- A00.9 Холера неуточненная
- K56.6 Другая и неуточненная кишечная непроходимость
- R11 Тошнота и рвота
- Z100* КЛАСС XXII Хирургическая практика
Фармакологическое действие
—
гидратирующее, дезинтоксикационное, нормализующее КЩС, плазмозамещающее.
Характеристика
Белые кубические кристаллы или белый кристаллический порошок соленого вкуса, без запаха. Легко растворим в воде (1:3), мало растворим в этаноле.
Фармакология
Натрия хлорид поддерживает соответствующее осмотическое давление плазмы крови и внеклеточной жидкости. При снижении концентрации натрия хлорида в плазме крови вода переходит из сосудистого русла в межтканевую жидкость, при значительном дефиците возникают спазмы гладких мышц и судорожные сокращения скелетной мускулатуры, нарушаются функции нервной и сердечно-сосудистой систем.
Раствор натрия хлорида 0,9% изотоничен плазме крови человека и поэтому быстро выводится из сосудистого русла, лишь временно увеличивая объем циркулирующей жидкости. Гипертонические растворы (3–5–10%) применяются в/в и наружно. При наружной аппликации они способствуют выделению гноя, проявляют противомикробную активность, при в/в введении — усиливают диурез и восполняют дефицит ионов натрия и хлора.
Применение вещества Натрия хлорид
Раствор 0,9% — большие потери внеклеточной жидкости (в т.ч. токсическая диспепсия, холера, диарея, неукротимая рвота, обширные ожоги с сильной экссудацией), гипохлоремия и гипонатриемия с обезвоживанием, кишечная непроходимость, в качестве дезинтоксикационного средства; промывание ран, глаз, полости носа, для растворения и разведения различных лекарственных веществ и увлажнения перевязочного материала.
Гипертонический раствор — легочное, желудочное и кишечное кровотечение, в качестве вспомогательного осмотического диуретика при проведении форсированного диуреза, обезвоживание, отравление нитратом серебра, для обработки гнойных ран (местно), запор (ректально).
Противопоказания
Гипернатриемия, ацидоз, гиперхлоремия, гипокалиемия, внеклеточная гипергидратация; циркуляторные нарушения, угрожающие отеком мозга и легких; отек мозга, отек легких, острая левожелудочковая недостаточность, сопутствующая терапия ГК в больших дозах.
Ограничения к применению
Нарушение функции почек, сердечная недостаточность, артериальная гипертензия, периферические отеки, токсикоз беременных (для больших объемов изотонического раствора).
Побочные действия вещества Натрия хлорид
Ацидоз, гипергидратация, гипокалиемия.
Передозировка
Случаи передозировки не описаны.
Способ применения и дозы
Изотонический раствор — в/в, п/к, в клизмах, местно. Перед введением раствор нагревают до 36–38 °C. Доза определяется в зависимости от потери организмом жидкости, в среднем составляет 1 л/сут; при дегидратации и интоксикациях — до 3 л/сут. Скорость введения — 540 мл/ч; при необходимости — больше. 0,9% раствор натрия хлорида применяют для промывания ран, глаз, слизистой оболочки полости носа, увлажнения перевязочного материала.
Гипертонические растворы: 10% раствор — в/в (до 20 мл); 2–5% раствор — для промывания желудка; 5% раствор — в клизмах (100 мл) для стимуляции дефекации при запорах (либо до 3 л/сут 0,9% раствора); местно — для обработки гнойных ран.
Торговые названия с действующим веществом Натрия хлорид
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Аква-Риносоль |
от 63.00 до 63.00 |
| АкваМастер® |
от 238.00 до 327.00 |
| ЛинАква беби Средство для промывания и орошения полости носа для детей и взрослых |
от 209.00 до 398.00 |
| ЛинАква норм Средство для промывания и орошения полости носа для детей и взрослых |
от 398.00 до 398.00 |
| ЛинАква софт Средство для промывания и орошения полости носа для детей и взрослых |
от 429.00 до 429.00 |
| ЛинАква форте Средство для промывания и орошения полости носа для детей и взрослых |
от 398.00 до 398.00 |
| ЛинАква форте Средство для промывания и орошения полости рта и горла для детей и взрослых |
от 434.00 до 434.00 |
| Натрия хлорид |
от 43.10 до 732.00 |
| Натрия хлорид Браун |
от 502.30 до 605.00 |
| Натрия хлорид буфус |
от 71.80 до 144.00 |
| Натрия хлорид-СОЛОфарм |
от 56.00 до 1446.00 |
Состав
Действующее составляющее этого средства — натрия хлорид. Формула хлорида натрия – NaCl, это кристаллы белого цвета, которые быстро растворяются в воде. Молярная масса 58.44 г/моль. Код ОКПД — 14.40.1.
Физиологический раствор (изотонический) – это раствор 0,9%, в нем содержится 9 г натрия хлорида, до 1 л дистиллированной воды.
Гипертонический раствор хлорида натрия – это раствор 10%, в нем содержится 100 г хлорида натрия, до 1 л дистиллированной воды.
Форма выпуска
Производится раствор натрия хлорида 0,9%, который может содержаться в ампулах по 5 мл, 10 мл, 20 мл. Ампулы применяются с целью растворения лекарств для введения инъекции.
Также производится раствор натрия хлорида 0,9% во флаконах емкостью по 100, 200, 400 и 1000 мл. Их применение в медицине практикуется для применения наружно, проведения капельных вливаний внутривенно, проведения клизм.
Раствор натрия хлорида 10% содержится во флаконах емкостью 200 и 400 мл.
С целью перорального применения выпускаются таблетки по 0,9 г .
Производится также назальный спрей во флаконах по 10 мл.
Фармакологическое действие
Хлорид натрия – это препарат, который действует как регидратирующее и дезинтоксикационное средство. Лекарство способно восполнять в организме недостаток натрия при условии развития разнообразных патологий. Хлорид натрия также увеличивает количество жидкости, которая циркулирует в сосудах.
Такие свойства у раствора проявляются благодаря наличию в нем хлорид-ионов и ионов натрия. Они способны проникать сквозь мембрану клеток с помощью разных транспортных механизмов, в частности натрий-калиевого насоса. Важную роль натрий играет в процессе передачи сигналов в нейронах, также он задействован в процессе метаболизма в почках и в электрофизиологических процессах сердца человека.
Фармакопея свидетельствует, что хлорид натрия поддерживает во внеклеточной жидкости и плазме крови постоянное давление. При нормальном состоянии организма достаточное количество этого соединения попадает в организм с продуктами питания. Но при патологических состояниях, в частности, при рвоте, поносе, серьезных ожогах отмечается повышенное выделение из организма этих элементов. Как следствие, организм испытывает дефицит ионов хлора и натрия, вследствие чего кровь становится гуще, нарушаются функции нервной системы, кровоток, судороги, спазмы гладкой мускулатуры мышц.
Если в кровь своевременно вводится изотонический раствор натрия хлорида, применение его способствует восстановлению водно-солевого баланса. Но так как осмотическое давление раствора аналогичное давлению плазмы крови, в сосудистом русле надолго он не задерживается. После введения он быстро выводится из организма. Как следствие, через 1 час в сосудах задерживается не больше половины введенного количество раствора. Поэтому в случае кровопотери раствор не является достаточно эффективным.
Средство также имеет плазмозамещающие, дезинтоксикационные свойства.
При введении внутривенно гипертонического раствора отмечается усиление диуреза, восполнение дефицита хлора и натрия в организме.
Фармакокинетика и фармакодинамика
Выведение из организма происходит в основном через почки. Немного натрия выделяется с потом и с калом.
Показания к применению
Натрия хлорид — это физраствор, который применяется в случае потери организмом внеклеточной жидкости. Показан при состояниях, которые ведут к ограничению поступления жидкости:
- диспепсия при отравлении;
- рвота, диарея;
- холера;
- обширные ожоги;
- гипонатриемия или гипохлоремия, при которых отмечается обезвоживание организма.
Учитывая, что такое натрий хлорид, его применяют наружно с целью промывания ран, глаз, носа. Препарат применяется с целью увлажнения перевязок, для ингаляций, для лица.
Показано использование NaCl для проведения форсированного диуреза при запоре, отравлениях, при внутренних кровотечениях (легочных, кишечных, желудочных).
Обозначено также в показаниях к применению хлорид натрия, что это такое средство, которое применяется для разведения и растворения лекарств, которые вводятся парентерально.
Противопоказания
Противопоказано применение раствора при таких болезнях и состояниях:
- гипокалиемия, гиперхлоремия, гипернатриемия;
- внеклеточная гипергидратация, ацидоз;
- отек легких, отек мозга;
- острая левожелудочковая недостаточность;
- развитие циркуляторных нарушений, при которых существует угроза отека мозга и легких;
- назначение больших доз ГКС.
Осторожно раствор назначают людям, которые болеют артериальной гипертензией, периферическими отеками, декомпенсированной хронической сердечной недостаточностью, почечной недостаточностью в хронической форме, преэклампсией, а также тем, у кого диагностированы другие состояния, при которых происходит задержка натрия в организме.
Если раствор применяется в качестве растворяющего средства для других лекарств, следует учесть существующие противопоказания.
Побочные действия
При применении хлорида натрия могут развиться следующие состояния:
- гипергидратация;
- гипокалиемия;
- ацидоз.
Если препарат применяется правильно, то маловероятно развитие побочных эффектов.
Если раствор NaCl 0.9% применяется как базовый растворитель, то побочные явления определяются свойствами лекарств, которые разводятся раствором.
При проявлении любых негативных эффектов нужно сразу сообщить об этом специалисту.
Инструкция по применению Натрия Хлорида (Способ и дозировка)
Инструкция на физ раствор (изотонический раствор) предусматривает его введение внутривенно и подкожно.
В большинстве случаев практикуется внутривенное капельное введение, для чего капельница Хлорида Натрия прогревается до температуры 36-38 градусов. Объем, который вводят пациенту, зависит от того, в каком состоянии пациент, а также от того количества жидкости, которая была потеряна организмом. При этом важно учесть возраст человека и его вес.
Средняя суточная доза препарата — 500 мл, вводится раствор со средней скоростью 540 мл/ч. Если отмечается сильная степень интоксикации, то максимальный объем лекарства в сутки может составлять 3000 мл. Если существует такая необходимость, можно вводить объем 500 мл на скорости 70 капель в минуту.
Детям вводится доза от 20 до 100 мл в сутки на 1 кг веса. Дозировка зависит от массы тела, от возраста ребенка. Следует учитывать, что при продолжительном применении этого лекарства необходимо обязательно контролировать уровень электролитов в плазме и моче.
Чтобы развести препараты, которые нужно вводить капельно, применяется от 50 до 250 мл натрия хлорида на одну дозу лекарства. Определение особенностей введения проводится по основному лекарству.
Введение гипертонического раствора проводится внутривенно струйно.
Если раствор применяется с целью немедленного восполнения дефицита ионов натрия и хлора, вводится капельно 100 мл раствора.
Чтобы провести ректальную клизму для вызывания дефекации, вводят 100 мл 5% раствора, также можно ввести на протяжении суток 3000 мл изотонического раствора.
Применение гипертонической клизмы медленно показано при почечных и сердечных отеках, повышенном внутричерепном давлении и при гипертонии проводится медленно, вводится 10-30 мл. Нельзя проводить такую клизму при эрозии толстой кишки и воспалительных процессах.
Гнойные раны раствором проводят согласно с той схемой, которую назначает врач. Компрессы с NaCl прикладывают непосредственно к ране или другому поражению на коже. Такой компресс способствует отделению гноя, гибели патогенных микроорганизмов.
Назальный спрей закапывают в полость носа после ее очищения. Взрослым пациентам закапывают по две капли в каждую ноздрю, детям – по 1 капле. Применяется как для лечения, так и для профилактики, для чего капают раствор на протяжении примерно 20 дней.
Натрия хлорид для ингаляций применяется при простудных заболеваниях. Для этого раствор смешивают с бронхолитическими препаратами. Ингаляция проводится на протяжении десяти минут трижды в день.
При крайней необходимости физраствор можно приготовить в домашних условиях. Для этого полную чайную ложку поваренной соли нужно размешать в одном литре кипяченной воды. При необходимости приготовить определенного количество раствора, например, с солью массой 50 г, следует провести соответствующие измерения. Такой раствор можно применять местно, использовать для клизм, полосканий, ингаляций. Однако ни в коем случае нельзя такой раствор вводить внутривенно или использовать для обработки открытых ран или глаз.
Передозировка
При передозировке пациент может чувствовать тошноту, страдать от рвоты и диареи, у него могут развиваться боли в животе, лихорадка, учащенное сердцебиение. Также при передозировке могут повышаться показатели артериального давления, развиваться отек легких и периферические отеки, почечная недостаточность, судороги мышц, слабость, головокружение, генерализованные судороги, кома. При чрезмерном введении раствора может развиться гипернатриемия.
При чрезмерном поступлении в организм может развиться гиперхлоримический ацидоз.
Если натрия хлорид применяется для растворения лекарств, то в основном передозировка связана со свойствами тех препаратов, которые подвергаются разведению.
При непреднамеренном избыточном введении NaCl важно прекратить этот процесс и оценить, есть ли негативнее симптомы у пациента. Практикуется симптоматическое лечение.
Взаимодействие
NaCl совмещается с большинством лекарств. Именно это его свойство обуславливает применение раствора для разведения и растворения ряда препаратов.
При разведении и растворении нужно обязательно контролировать совместимость препаратов визуально, определяя, не появляется ли в процессе осадок, не меняется ли цвет и др.
Плохо совмещается с норадреналином.
При одновременном назначении препарата с кортикостероидами важно постоянно отслеживать содержание электролитов в крови.
При параллельном приеме понижается гипотензивное действие Эналаприла и Спираприла.
Несовместим Натрия Хлорид со стимулятором лейкопоэза Филграстимом, а также с полипептидным антибиотиком Полимиксин В.
Есть данные о том, что изотонический раствор увеличивает биодоступность лекарств.
При разведении раствором порошкообразных антибиотиков они усваиваются организмом полностью.
Условия продажи
В аптеках продается по рецепту. При необходимости применения препарата для разбавления других лекарств и т.п. выписывают рецепт на латинском языке.
Условия хранения
Хранить порошок, таблетки и раствор нужно в сухом месте, в хорошо закупоренной таре, при этом температура должна составлять не более 25 градусов Цельсия. Важно беречь препарат от доступа детей. Если упаковка герметична, то замораживание не влияет на свойства препарата.
Срок годности
Для хранения порошка и таблеток ограничений нет. Раствор в ампулах 0,9% может храниться на протяжении 5 лет; раствор во флаконах 0,9% – один год, раствор во флаконах 10%– 2 года. Нельзя использовать после того, как срок хранения завершился.
Особые указания
Если проводится инфузия, нужно тщательно следить за состоянием пациента, в частности, за электролитами плазмы крови. Следует учитывать, что у детей ввиду незрелости функции почек возможно замедление экскреции натрия. Важно определить его концентрацию в плазме перед проведением повторных инфузий.
Важно контролировать состояние раствора перед его введением. Раствор должен быть прозрачным, упаковка – неповрежденной. Применять раствор для внутривенного введения может только квалифицированный специалист.
Растворять любые препараты Натрием Хлорида должен только специалист, который может квалифицированно оценить, является ли полученный раствор пригодным для введения. Важно строго выдерживать все правила антисептики. Введение любого раствора нужно проводить сразу же после его приготовления.
Итогом ряда химических реакций с участием натрия хлорида является образование хлора. Электролиз расплава Хлорида Натрия в промышленности – способ получения хлора. Если провели электролиз раствора Хлорида Натрия, также в итоге получают хлор. Если на кристаллический Хлорид Натрия подействовали серной кислотой концентрированной, в итоге получают хлороводород. Сульфат натрия и гидроксид натрия можно получить путем цепочки химических реакций. Качественная реакция на хлорид ион – реакция с нитратом серебра.
Аналоги
Совпадения по коду АТХ 4-го уровня:
У разных производителей лекарственных средств раствор может выпускаться под отдельным названием. Это препараты Натрия хлорид Браун, Натрия хлорид Буфус, Ризосин, Салин Натрия хлорид Синко и др.
Также производятся препараты, вмещающие в составе хлорид натрия. Это комбинированные солевые растворы натрия ацетат + натрия хлорид и др.
Детям
Применяется согласно с инструкцией и под тщательным контролем специалистов. Следует учитывать незрелость функции почек у детей, поэтому повторное введение проводится только после точного определения уровня натрия в плазме.
При беременности и лактации
При беременности капельница с хлоридом натрия может применяться только при патологических состояниях. Это токсикоз в средней или тяжелой стадии, а также гестоз. Здоровые женщины получают натрий хлорид с пищей, причем, его избыток может привести к развитию отеков.
Отзывы
Большинство отзывов – положительные, так как пользователи пишут об этом средстве, как о полезном препарате. Особенно много отзывов о назальном спрее, который, по мнению пациентов, является неплохим средством как для профилактики, так и для лечения насморка. Средство эффективно увлажняет слизистую носа и способствует выздоровлению.
Цена Натрия Хлорида, где купить
Цена физ раствора в ампулах по 5 мл составляет в среднем 30 рублей за 10 шт. Купить натрия хлорид 0,9% во флаконе 200 мл составляет в среднем 30-40 рублей за 1 флакон.
- Интернет-аптеки РоссииРоссия
ЗдравСити
-
Натрия хлорид раствор для инъекций 0,9% 10мл 10штОАО Дальхимфарм
-
Натрия хлорид буфус раствор для инъекций 0,9% 5мл 10штАО Обновление ПФК
-
Натрия хлорид раствор для ин. 0,9% 10мл 10штАО Обновление ПФК
-
Натрия хлорид раствор для инф. 0,9% 200мл 24 штПАО Биосинтез
Аптека Диалог
-
Натрия хлорид (фл. 0,9% 400мл)Эском
-
Натрия хлорид (амп. 0,9% 5мл №10)Гротекс ООО
-
Натрия хлорид (амп. 0,9% 5мл №10)ДХФ ОАО
-
Натрия хлорид (амп. 0,9% 10мл №10)Фармасинтез
-
Натрия хлорид (фл. 0,9% 200мл (пластик))Гротекс ООО
показать еще
Справочник содержит названия веществ и описания химических формул (в т.ч. структурные формулы и скелетные формулы).
Хлорид натрия
Брутто-формула:
ClNa
Названия
Русский:
- Хлорид натрия(IUPAC)
- галит
- каменная соль
- натрия хлорид
- обычная соль
- пищевая соль
- поваренная соль
- столовая соль
English:
- Common salt
- Halite
- Rock salt
- Saline
- Sodium chloric
- Sodium chloride(IUPAC)
- Table salt
Варианты формулы:
Реакции, в которых участвует Хлорид натрия
-
2{M} + {Hal}2 = 2{M}{Hal}
, где M =
Li Na K Rb Cs; Hal =
F Cl Br I -
2NaCl + 2H2O «e-«-> 2NaOH + Cl2″|^» + H2″|^»
-
ZnCl2 + 4NaOH «90^oC»—> Na2[Zn(OH)4] + 2NaCl
-
Na2[Zn(OH)4] + 2HCl -> 2NaCl + Zn(OH)2″|v» + 2H2O
-
Na2[Zn(OH)4] + 4HCl -> 2NaCl + ZnCl2 + 4H2O
Натрий хлорид
Оглавление раздела
Оптовые поставки • Свойства вещества • Транспортировка • Получение • Применение • Безопасность • Производитель • Заказать

Торговое наименование фармацевтической субстанции Натрия хлорид
Международное непатентованное, группировочное или химическое наименование Натрия хлорид
Физическое состояние Субстанция-порошок
Внешний вид Белый кристаллический порошок или крупинки или бесцветные кристаллы
Оптовые поставки хлорида натрия
Наш завод по производству химических реагентов, производит хлорид натрия в любых объемах. Так же Вы можете заказать его доставку, в каком бы городе России Вы ни находились, товар дойдет в полной сохранности, т.к. мы используем только тару по ГОСТу.
Сделав заказ натрия хлорида партии любого объема, Вы получите продукт вовремя и должного качества, с отгрузкой прямо с нашего завода без посреднических наценок и других издержек. Чистое вещество напрямую от российского производителя.
Свойства хлорида натрия
Хлорид натрия с обозначением химической формулы как NaCl — представляет из себя натриевую соль соляной кислоты. Этот химический элемент называют еще как поваренная соль, или как обычная соль, которую используют широко в кулинарии и которая знакома каждой домохозяйке. Хлорид натрия в большом количестве содержится в морской воде, из которой ее активно добывают. А уже чистый хлорид натрия имеет вид бесцветных кристаллов.

Кристаллы хлорида натрия под микроскопом
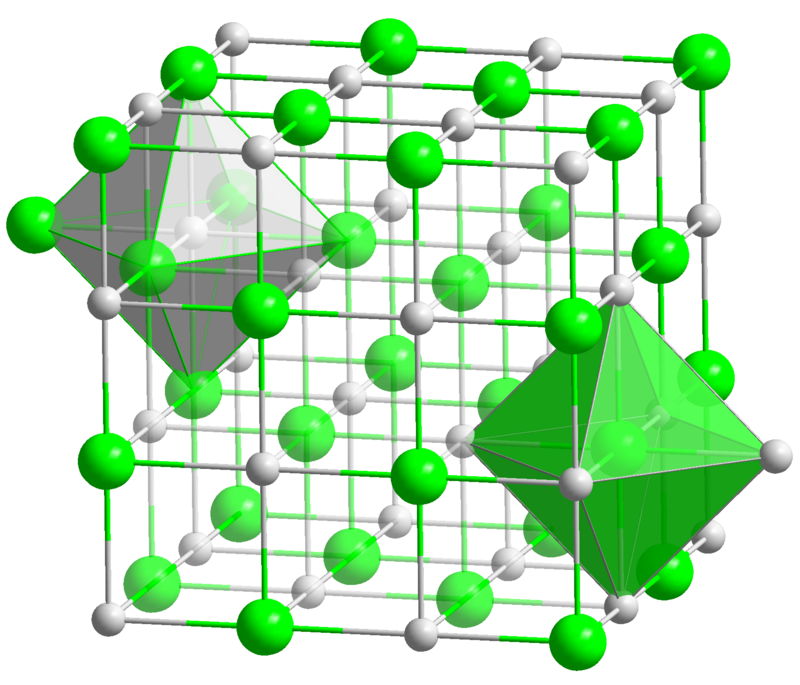
Схема строения молекул вещества
Окраска раствора должна измениться от прибавления не более 0,5 мл 0,01 М раствора натрия гидроксида или не более 0,5 мл 0,01 М раствора хлористоводородной кислоты
| Показатели качества | |
| Наименование показателя | Требования ФСП |
| 1. Описание | Белый кристаллический порошок или крупинки, или бесцветные кристаллы |
| 2. Растворимость | Легко растворим в воде, мало растворим в спирте 96% |
| 3. Подлинность | Дает характерные реакции на натрий и хлориды |
| 4. Прозрачность раствора | Должен быть прозрачным |
| 5. Цветность раствора | Должен быть бесцветным |
| 6. Кислотность или щелочность | Окраска раствора должна измениться от прибавления не более 0,5 мл 0,01 М раствора натрия гидроксида или не более 0,5 мл 0,01 М раствора хлористоводородной кислоты |
| Щелочноземельные металлы и магний | Не более 0,01% в пересчете на кальций |
| 8. Барий | Мутность раствора субстанции не должна превышать мутность эталонного раствора |
| 9. Железо, %, не более | 0,0003 |
| 10. Тяжелые металлы, %, не более | 0,0005 |
| 11. Сульфаты, %, не более | 0,005 |
| 12. Калий, %, не более | 0,05 |
| 13. Соли аммония, %, не более | 0,004 |
| 14. Потеря в массе при высушивании, %, не более | 0,5 |
| 15. Мышьяк, %, не более | 0,00005 |
| 16. Фосфаты, %, не более | 0,0025 |
| 17. Бромиды, %, не более | 0,005 |
| 18. Иодиды | Раствор не должен окрашиваться в голубой цвет |
| 19. Ферроцианиды | Раствор не должен окрашиваться в голубой цвет |
| 20. Микробиологическая чистота | Категория 1.2.Б |
| 21. Количественное определение (NaCl), %, в пределах | Не менее 99,5% NaCl в пересчете на сухое вещество |
| 22. Бактериальные эндотоксины, предельное содержание не более | Не более 5 ЕЭ на 1 г субстанции |
| Упаковка | По 1 кг, 3 кг, 5 кг в полипропиленовые пакет из полиэтиленовой пленки, который термосваривают двумя швами, снабжая внутренней этикеткой. Пакеты укладывают в тканый полипропиленовый мешок с внутренним полиэтиленовым пакетом и прошивают вместе с этикеткой. По 25 кг – в тканый полипропиленовый мешок с внутренним полиэтиленовым пакетом Полиэтиленовый пакет термосваривают, полипропиленовый мешок прошивают. Каждая упаковка снабжена этикеткой. Этикетка из этикеточной бумаги, писчей, офсетной. |
| Маркировка | В соответствии с нормативной документацией |
| Хранение | В сухом месте при температуре не выше 250С |
| Срок годности | 5 лет |
Не более 5 ЕЭ на 1 г субстанции
| Общие свойства | |
|---|---|
| Систематическое наименование |
Хлорид натрия |
| Традиционные названия | Соль, поваренная соль, столовая соль, пищевая соль, каменная соль, галит |
| Хим. формула | NaCl |
| Физические свойства | |
| Молярная масса | 58,44277 г/моль |
| Плотность | 2,165 г/см³ |
| Термические свойства | |
| Температура плавления | 800,8 °C |
| Температура кипения | 1465 °C |
| Мол. теплоёмк. | 50,8 Дж/(моль·К) |
| Энтальпия образования | −234,8 кДж/моль |
| Удельная теплота испарения | 170,85 кДж/моль |
| Удельная теплота плавления | 28,68 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 35,6 г/100 мл (0 °C) 35,9 г/100 мл (+25 °C) 39,1 г/100 мл (+100 °C) |
| Растворимость в метаноле | 1,49 г/100 мл |
| Растворимость в аммиаке | 21,5 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,544202 (589 нм) |
| Структура | |
| Координационная геометрия | Октаэдральная (Na +) Октаэдральная (Cl -) |
| Кристаллическая структура | гранецентрированная кубическая, cF8 |
| Классификация | |
| Рег. номер CAS | 7647-14-5 |
| PubChem | 5234 |
| Рег. номер EINECS | 231-598-3 |
| SMILES | [Na+].[Cl-] |
| InChI | InChI=1S/ClH.Na/h1H;/q;+1/p-1 FAPWRFPIFSIZLT-UHFFFAOYSA-M |
| RTECS | VZ4725000 |
| ChEBI | 26710 |
| ChemSpider | 5044 |
| Безопасность | |
| ЛД50 | 3000–8000 мг/кг |
| NFPA 704 |
Транспортировка
Наш завод предоставляет гарантию на хранение вещества при должном соответствии требований, предъявляемые при правильной транспортировке и хранении.
Так как хлорид натрия требует к себе особого внимания при транспортировке, то нужно отнестись к его упаковке с особой тщательностью. Вообще, разработаны ГОСТы по его упаковке, и мы конечно, стараемся их соблюдать. Поэтому на нашем химическом заводе готовое вещество упаковываются в прочные полиэтиленовые мешки, которые в свою очередь завязываются двойным узлом нитью (или запаиваются). После этого возможна дополнительная упаковка в в фанерные коробы или в картонные. Или, на выбор покупателя, так же возможна упаковка этого вещества в бумажные пяти-шести-слойные мешки.
Получение
Хлорид натрия добывается из естественных природных источников, обычно к ним относятся залежи галита, осадочной горной породы в виде каменной соли ну и конечно же он содержится в огромном количестве в морской воде, из которой ее просто выделяют методом выпаривания
Применение
Для приготовления стерильных (инъекционных) лекарственных форм
В фармацевтике изотонический раствор хлорида натрия применяется как средство для дезинтоксикации, а так же в качестве растворителя каких либо других лекарственных средств. А так же при многих других ситуациях — как гипертонический раствор, вспомогательный осмотический диуретик, так же используется для поднятия давления при кровотечениях, при отравлении нитратом серебра, а так же для обработки гнойных ран и при отечностях в качестве наружного средства.
Как видно из описания, данный химический элемент довольно распространен в медицинской области. Но он так же активно применяется чуть ли не повсеместно и в промышленности и быту.
Применение

А так же имеем собственный автотранспорт, специально приспособленный для перевозки химических веществ на дальние расстояния.
При заключении долговременного на поставки продукции с нашего химического предприятия, для Вас начинают действовать особые цены, которые помогут сделать общение с нами еще более выгодным.
Хлорид калия оптом доступен для отгрузки с нашего склада, в любых количествах, в различных фасовках по самым выгодным ценам от Российского производителя. Предоставляем готовые ТУ, а также разрабатываем новые — под ваши конкретные запросы.
Безопасность
Изза того что вещество само по себе практически безопасно для человека, само собой в умеренных количествах, особые меры предосторожности не обязательны.
В помещениях где активно ведется работа с хлорид натрием, у рабочих должны быть маски (респираторы) и защитные очки. При попадании вещества в глаза, обильно промыть водой. При вдыхании большого количества пыли, выйти на свежий воздух, продышаться.
Среди экологических меры предосторожности есть рекомендации держать вещество подальше от канализации, поверхностных и грунтовых вод.
Производитель натрий хлорида

МЗХР обладает всем необходимым, что бы выполнить любой заказ точно по техническим условиям заказчика и, что не маловажно, в нужный временной интервал.
Вот какие преимущества позволяют нам этого добиться:
- собственный ж/д тупик, благодаря которому возможно отправить продукцию в любую точку Европы или Азии, а так же ближнего востока;
- контроль качества производства, имеется собственная лаборатория;
- Надежное и проверенное оборудование, которое позволяет произвести большие объемы за короткое время;
- наличие больших запасов сырья;
- собственные склады;
- свой автотранспорт.
Михайловский завод химических реагентов — российский прямой поставщик натрий хлорида на рынки Росии и СНГ, а так же некоторых зарубежных государств. Географически расположенный приблизительно в центре России — в Алтайском крае, дает нам преимущество по отправке продукции как на запад, так и на восточные направления.
Поэтому, если Вы искали производителя натрий хлорида именно в России, то стоит узнать все условия по работе с нами, возможно наш завод будет полностью удовлетворять Ваши потребности в этом веществе долгие годы.


![{displaystyle {ce {2 NaCl + 2 H2O ->[electrolysis] Cl2 + H2 + 2 NaOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6175336b0ecf3b2032d6a60ac2a534b10e6f61f3)